El ARN de los coronavirus codifica poliproteínas que se escinden en varias proteínas responsables de su replicación en la célula huésped. Las proteasas que producen la escisión son dianas terapéuticas preferentes para los fármacos antivirales. La proteasa principal (Mpro), también llamada proteinasa tipo-3C (3CLpro), del coronavirus SARS-CoV-2 se encuentra en la poliproteína ORF1ab. Se ha publicado la estructura tridimensional de este dímero con una resolución de 1.75 Å usando cristalografía de rayos X. Se confirma su gran semejanza con la de SARS-CoV (que se publicó en 2003), como predecían los modelos teóricos basados en homología (la gran semejanza entre sus secuencias de aminoácidos). Además, se ha usado esta estructura para buscar nuevos antivirales usando herramientas bioinformáticas.
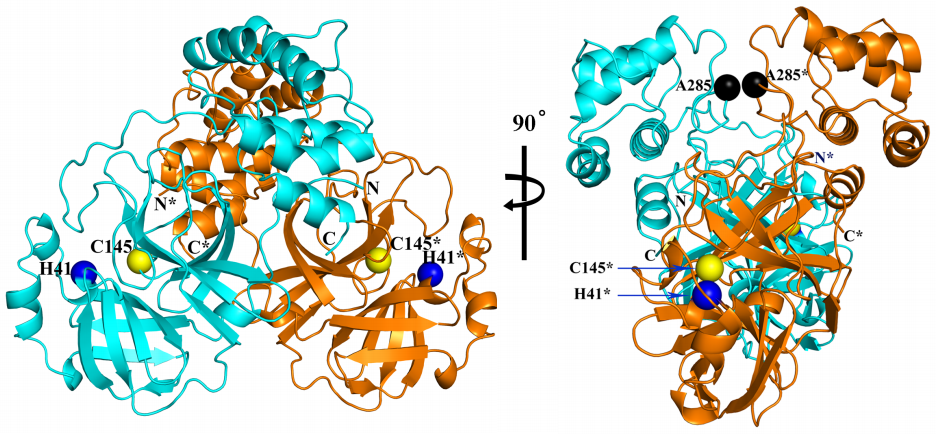
Solo 12 aminoácidos diferencian la proteasa principal de SARS-CoV-2 (COVID-19) y la de SARS-CoV (SARS); parece que dos de ellas, A285T y L286I, están relacionadas con una capacidad de infectar 3.6 mayor para el nuevo coronavirus. El cambio A285T permite que dos dominios se aproximen un poco más entre sendas proteínas del dímero; en concreto, la distancia entre los átomos de calcio de los residuos en la posición 285 se encuentran a 6.77 Å en la proteína Mpro de SARS-CoV mientras se acercan hasta 5.21 Å en Mpro de SARS-CoV-2; así los centros de los dominios a los que pertenecen se acercan de 33.4 Å hasta 32.1 Å. Parece que esta diferencia tiene gran relevancia en la búsqueda de antivirales más eficaces.
Se están usando herramientas bioinformáticas para cribar (buscar) fármacos contra la proteasa principal de SARS-CoV-2 (en especial, los que se puedan reposicionar, que permiten acelerar los estudios clínicos). Por ejemplo, Anh-Tien Ton, Francesco Gentile, …, Artem Cherkasov, “Rapid Identification of Potential Inhibitors of SARS‐CoV‐2 Main Protease by Deep Docking of 1.3 Billion Compounds,” Molecular Informatics (11 Mar 2020),
Por cierto, las simulaciones por dinámica molecular parecen indicar que los inhibidores de Mpro que son moléculas pequeñas parecen ser ineficaces, recomendándose moléculas más grandes. Más información en Maria Bzówka, Karolina Mitusińska,
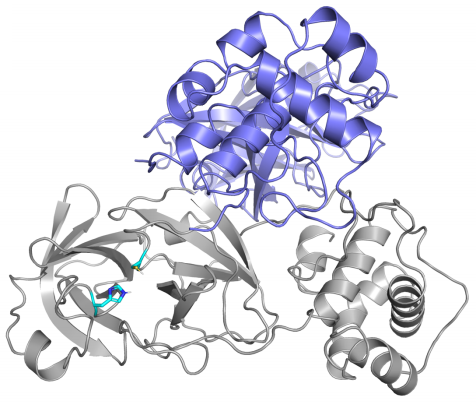
Esta es la primera reconstrucción por ordenador de la proteasa principal de SARS-CoV-2 que se publicó (según me consta); está basada en su homología con SARS-CoV. Aunque en la primera figura de esta pieza aparece el dímero (formado por dos copias de la proteína) que se ha cristalizado y aquí solo se presenta el monómero, se puede comprobar que son muy similares entre sí. Por fortuna, pues varios artículos posteriores se han basado en ella para estudiar el efecto de algunos fármacos inhibidores de su actividad.
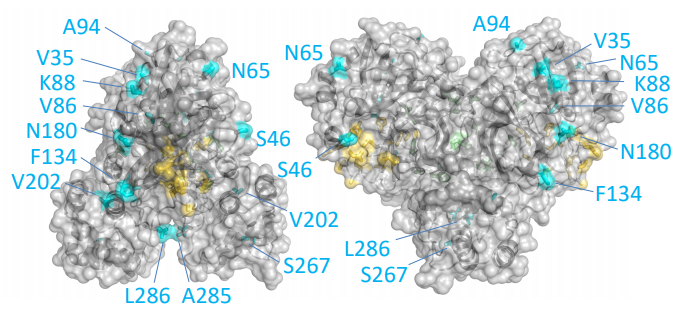
Esta reconstrucción de la proteasa principal (Mpro) del coronavirus SARS-CoV-2 muestra coloreados en celeste los residuos (aminoácidos) diferentes con dicha proteína de SARS-CoV. Solo se diferencian en 12 aminoácidos: V35L, S46A, N65S, V86L, K88R, A94S, F134H, N180K, V202L, S267A, A285T, y L286I; repito lo que ya dije más arriba, para quienes no conozcan la notación, por ejemplo, F134H (Phe134His) significa que SARS-CoV-2 tiene una F (Phe o fenilalanina) en la posición 134 de su secuencia de aminoácidos, donde SARS-CoV tiene una H (His o histidina), y así con todos los demás (
tabla de aminoácidos). Puedes consultar las secuencias de referencia
NP_828863.1 (SARS-CoV) y
YP_009725301.1 (SARS-CoV-2).
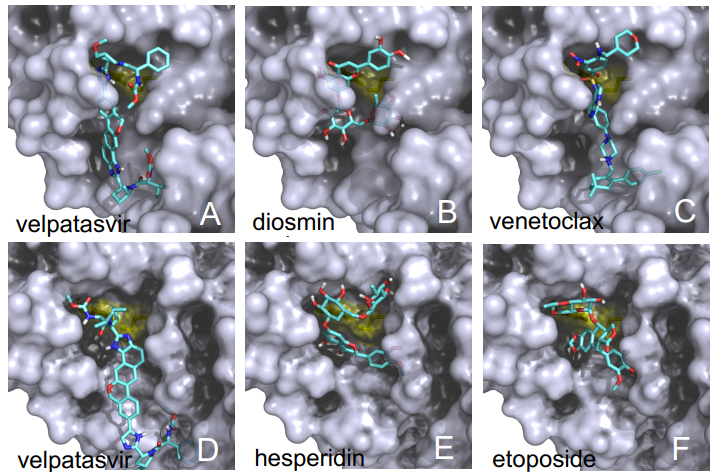
Las diferencias entre proteasa principal de SARS-CoV-2 y SARS-CoV son tan pequeñas que podemos confiar en la reconstrucción por homología de su estructura tridimensional. Gracias a ello podemos estudiar cómo interaccionan con esta proteasa diferentes antivirales, tanto los que atacan la cadena A (velpatasvir, diosmin y venetoclax) como los que atacan la cadena B (velpatasvir, hesperidin y etoposide). Por supuesto hay muchos más antivirales que inhiben esta proteasa, los de la figura son solo unos ejemplos representativos.
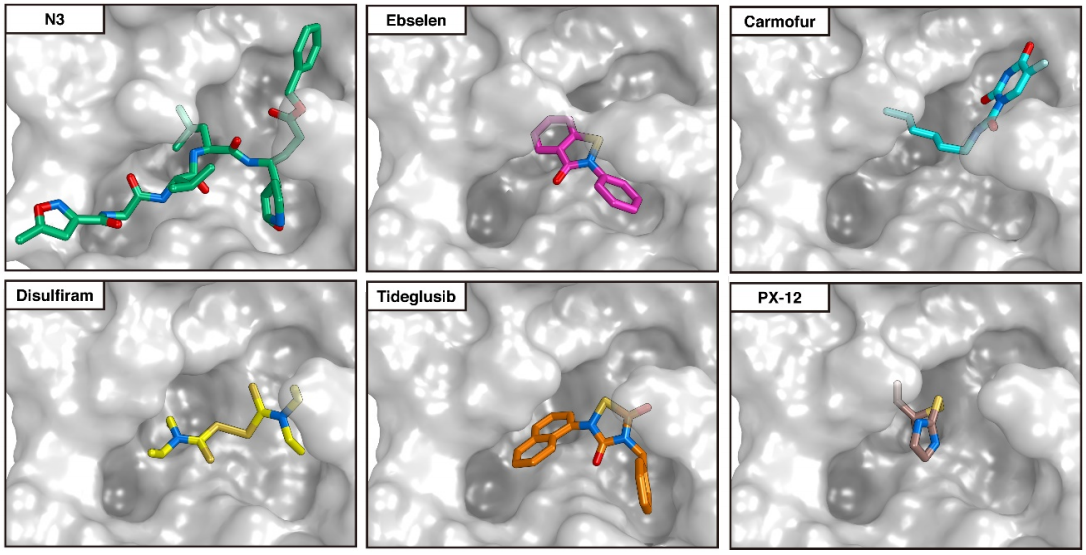
Esta figura muestra la predicción para la colocación (
docking pose) de otros seis inhibidores de la proteasa principal en su sitio de acción. En concreto, N3, ebselen, carmofur, disulfiram, tideglusib y PX-12. Se han estudiado muchos más y se han realizado diferentes comparaciones entre ellos; por lo que parece son más eficaces las moléculas más grandes que parecen inhibir de forma más completa el sitio activo de la proteasa.
En resumen, se está trabajando mucho en el desarrollo de inhibidores de la proteasa principal del coronavirus SARS-CoV-2. Muchos se están probando en diferentes ensayos clínicos (alguno incluso usan varios en cócteles). En los próximos meses se publicarán los resultados (algunos serán prometedores, otros serán decepcionantes), pero auguro que antes de finales de año tendremos varias terapias exitosas ya ensayadas contra COVID-19. Las vacunas tardarán más en llegar, pero creo que son menos urgentes. La ciencia, como siempre, dando respuestas a velocidad de vértigo, aunque todo el mundo sueña con que lo hiciera a velocidad superlumínica, algo imposible.
Y QUE ÉSTA LA INTERNALIZARA. Todo eso, junto a una FUERTE INTERNALIZACIÓN DE VALORES PATRIOS, no sé si lo hubiera eliminado pero si creo que, hubiera atenuado esa tendencia weona antisocial de "ser pillo" cagándose a los demás
Así como tampoco mató a todos los comunachos
¡PINOCHO AWEONAO!