impedancibolivariano
Animal
- Registrado
- 2020/09/12
- Mensajes
- 2.276
- Sexo

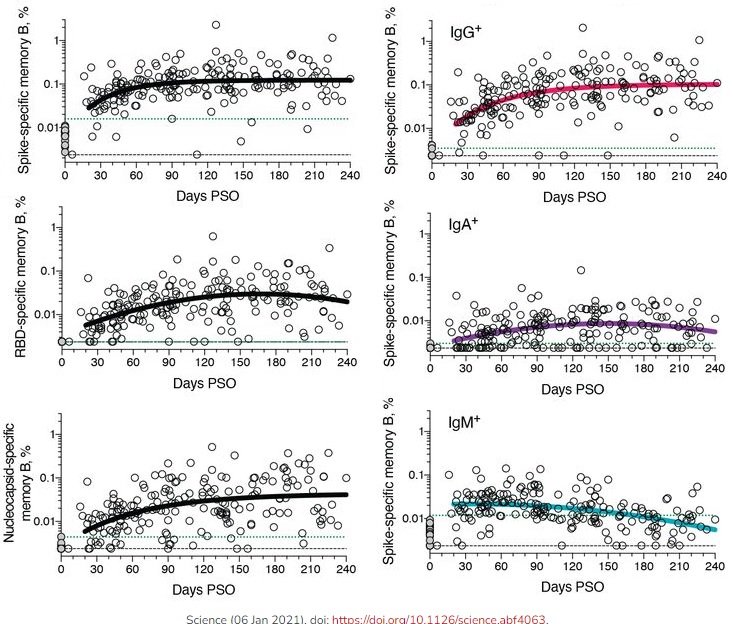
La evolución de la memoria inmunitaria tras superar la COVID-19 es un tema que despierta gran interés. Se publican en Nature y Science sendos artículos que observan que los linfocitos B mantienen sus títulos y retienen su capacidad de producir anticuerpos contra futuras reinfecciones hasta 191 días (6.2 meses) y hasta 240 días (8 meses), respectivamente. Estos estudios de la respuesta inmunitaria celular y humoral aparecieron como preprints en bioRxiv en noviembre de 2020, generando cierto eco mediático (entonces el de Science solo alcanzaba 6 meses). En Nature se estudia a 87 personas (se excluyeron 13 de las 100 iniciales) y en Science a 188 (108 mujeres). Todo apunta a que la memoria inmunitaria contra el SARS-CoV-2 en los linfocitos B es duradera (quizás incluso sea permanente), en la línea de la inmunidad contra el SARS-CoV-1 que se sabe que supera los 17 años. Buenas noticias para la eficiencia de las vacunas eficaces.
Ambos trabajos también han explorado la respuesta inmunitaria humoral, los anticuerpos IgM, IgG y IgA contra el dominio de unión al receptor (RBD) de la espícula (proteína S) y la nucleocápside (proteína N) del SARS-CoV-2. El artículo de Science observa que los anticuerpos IgG y IgA se mantienen casi constantes hasta los seis meses, pero los IgM decrecen de forma significativa. El artículo de Nature observa que los anticuerpos IgM e IgG decrecen mucho, mientras que los IgA decrecen mucho menos. En ambos casos, lo más relevante es la respuesta inmunitaria celular. En cuanto a los linfocitos T CD4+ (colaboradores) y los linfocitos T CD8+ (citotóxicos) sus títulos decrecen y su vida media está entre 3 y 5 meses. Así, cada componente del sistema inmunitario tiene una cinética (evolución en el tiempo) diferente tras la infección con COVID-19.
Por cierto, el artículo de Nature presenta el resultado de biopsias mostrando la persistencia de ARN del SARS-CoV-2 en el intestino delgado de pacientes (incluso en los asintomáticos); en la primera versión del preprint en bioRxiv también se mostraban imágenes con coronavirus en estas biopsias, pero como no se logró demostrar que fueran de SARS-CoV-2 se eliminaron en el artículo de Nature (es lo que tiene la revisión por pares). El papel de los reservorios intestinales del coronavirus tendrá que ser explorado en futuras investigaciones, pero podría ser relevante en la persistencia de la memoria inmunitaria.
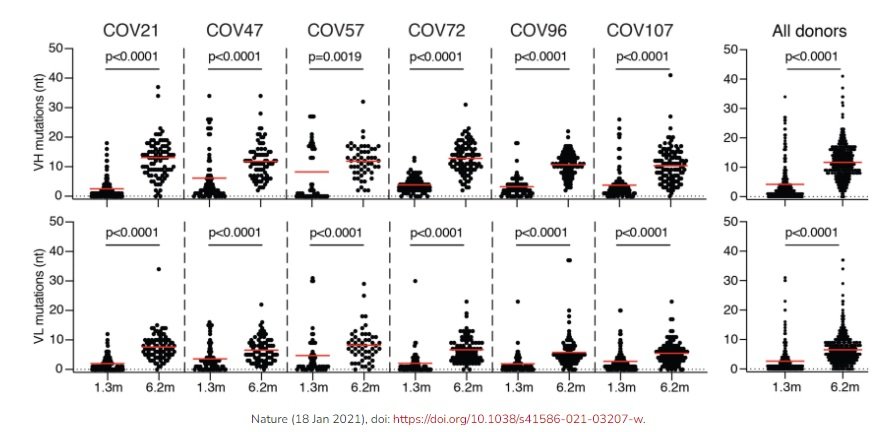
La memoria inmunitaria celular en los linfocitos B se estudia mediante citometría de flujo a partir de muestras de plasma de los pacientes. El artículo de Nature muestra que el porcentaje de linfocitos B de memoria que producen anticuerpos contra el RBD de la espícula crece marginalmente entre 1.3 y 6.2 meses. Esta figura muestra el cambio para cinco clones (COV21, COV47, COV57, COV72, COV96 y COV107) de los 122 estudiados para los idiotipos VL y VH (las dos regiones variables de la región en V de las IgG, o inmunoglobulinas G); recuerda que los linfocitos B son policlonales y maduran dando lugar a clones que son específicos para diferentes antígenos. Se ha observado que 43 de los clones presentes a los 1.3 meses no eran detectables a los 6.2 meses, mientras que se observaron 22 nuevos clones; se interpreta este resultado como indicación de que existen restos del coronavirus en los pacientes que siguen dando lugar a respuesta inmunitaria celular.
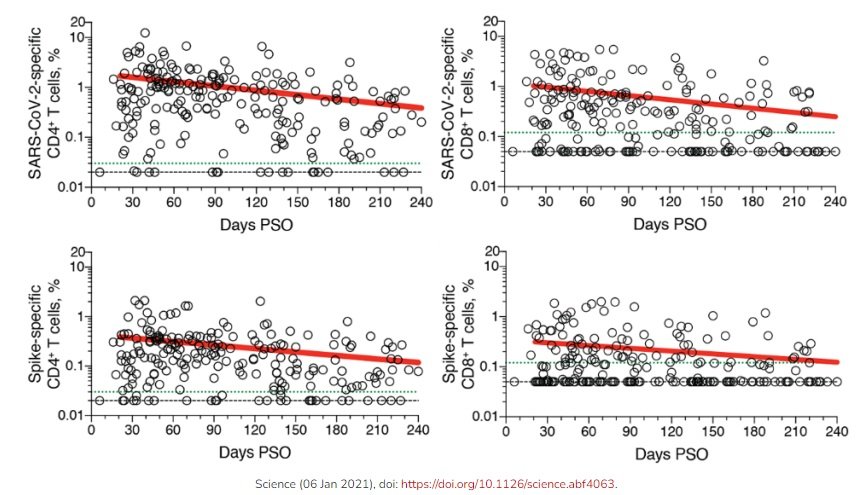
El artículo en Science muestra que los títulos de los linfocitos T CD4+ (colaboradores) y CD8+ (citotóxicos) decrecen con el tiempo. La proporción de individuos con CD8+ después de los 6 meses fue de solo el 50 %, mientras que con CD4+ fue del 92 %; así los resultados para los CD8+ podrían estar subestimados. Aún así no me resisto a detallarlos: la vida media de los CD8+ específicos del SARS-CoV-2 (proteínas S, M, N y ORF3a) es de t1/2 = 125 días (R = −0.24, p = 0.0003), aunque solo para los específicos de la espícula (proteína S) es de t1/2 = 225 días (R = −0.18, p = 0.007); mientras la vida media de los CD4+ específicos del SARS-CoV-2 es de t1/2 = 94 días (R = −0.29, p<0.0001), y la de los específicos de la espícula es de t1/2 = 139 días (R = −0.26, p<0.0001).
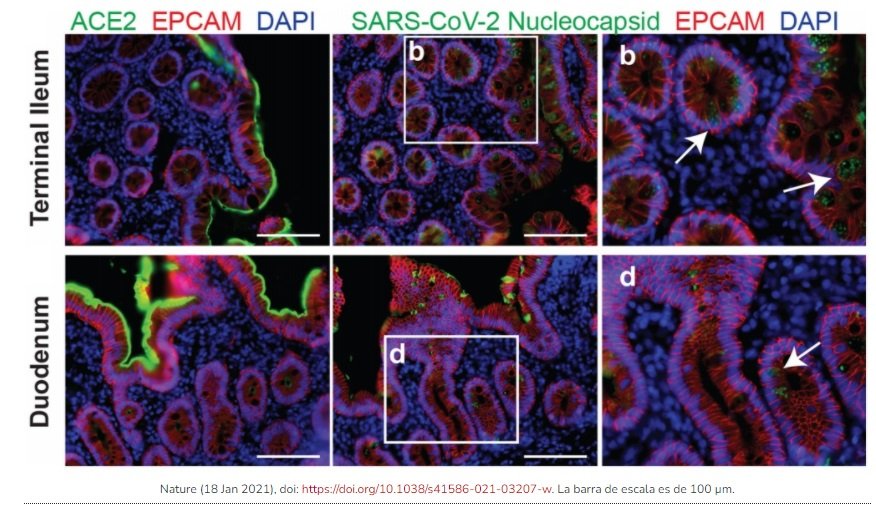
El artículo de Nature presenta imágenes por inmunofluorescencia de biopsias de tejido de la nasofaringe y del intestino delgado de 14 pacientes muestran la presencia de antígenos durante al menos 4 meses (las biopsias se realizaron entre 2.8 y 5.7 meses tras la infección). En 5 de los 14 pacientes se detectó el receptor ACE2 humano y la proteína N de nucleocápside del SARS-CoV-2 en enterocitos intestinales (no se encontraron en las biopsias de los controles). En 3 de los 14 participantes se pudo usar la PCR (pues el número de ciclos Ct < 40) para verificar que era SARS-CoV-2. Así los resultados apoyan la hipótesis de que los complejos inmunes (antígeno-anticuerpo) se retienen en la superficie de las células dendríticas foliculares durante mucho tiempo; estos complejos actúan como fuente potencial de antígenos y podrían estar detrás del incremento con el tiempo de los títulos de los linfocitos B de memoria.
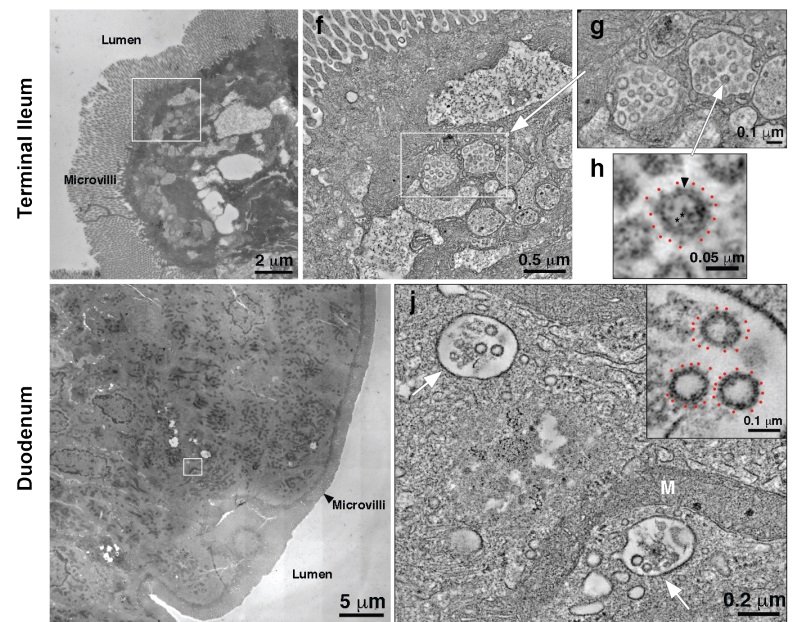
En la primera versión (v1) del preprint en bioRxiv se incluyen imágenes tomográficas que muestran la presencia de coronavirus encerrados en compartimentos dentro del citoplasma de los enterocitos en las biopsias del intestino (íleon y duodeno). Dichas imágenes han sido eliminadas de la segunda versión (v2) y del artículo publicado en Nature; la razón debe ser que no hay pruebas de que sean de SARS-CoV-2, pudiendo ser restos de otros coronavirus (en la revisión por pares es habitual solicitar pruebas adicionales que apoyen las hipótesis dudosas, que si no son aportadas requieren la eliminación de dichos resultados). Creo que es relevante recordar que muchos virus persisten durante mucho tiempo en ciertos tejidos del organismo (por ejemplo, el virus del Ébola se oculta en el fluido ocular durante más de un mes). No se puede descartar que el coronavirus SARS-CoV-2 también lo haga en el tejido intestinal y otros tejidos (algo que podría estar relacionado con la COVID-19 persistente). Por desgracia, no se sabe si estos viriones encapsulados dentro de los enterocitos son infectivos.
En resumen, la memoria inmunitaria inducida por la infección de la COVID-19 parece durar bastante tiempo (al menos 8 meses y probablemente mucho más). La memoria más duradera es la asociada a los epítopos de la espícula del coronavirus, una buena noticia para las vacunas que se basan en vehicular la proteína S para inducir esta memoria. Sin embargo, no se puede descartar que a medio o largo plazo las nuevas variantes del coronavirus acaben siendo nuevas cepas que escapen a esta memoria inmunitaria, permitiendo reinfecciones potenciales. Por ello es necesario vacunar cuanto antes a un alto porcentaje de la población susceptible a infección con objeto de contener el desarrollo y la expansión de nuevas variantes. Y no lo olvides, vacúnate cuando te llegue el turno sin dudarlo y mientras tanto recuerda que tienes que extremar las medidas para evitar contagiarte porque hasta entonces la vacuna eres tú.
Como comentario, les dejo el vidio explicando como la vacuna de Pfizer alcalza la respuesta inmunologica humoral y celular